Ətrafımızdakı təbiət hadisələri və prosesləri olduqca mürəkkəbdir. Onların dəqiq fiziki təsviri üçün çətin riyazi aparatdan istifadə edilməli və çoxlu sayda əhəmiyyətli amillər nəzərə alınmalıdır. Bu problemin qarşısını almaq üçün fizikada prosesin riyazi təhlilini xeyli asanlaşdıran, lakin onun təsvirinin düzgünlüyünə praktiki olaraq təsir göstərməyən bəzi sadələşdirilmiş modellərdən istifadə olunur. Onlardan biri ideal qaz modelidir. Bunu məqalədə daha ətraflı nəzərdən keçirək.
İdeal qaz anlayışı
İdeal qaz bir-biri ilə qarşılıqlı təsirdə olmayan maddi nöqtələrdən ibarət olan maddənin birləşmə vəziyyətidir. Gəlin bu tərifi daha ətraflı izah edək.
Birincisi, ideal qazı təşkil edən cisimlər kimi maddi nöqtələrdən danışırıq. Bu o deməkdir ki, onun molekulları və atomları ölçüyə malik deyil, müəyyən kütləyə malikdir. Cəsarətlidiraşağı təzyiq və yüksək temperaturda olan bütün real qazlarda molekullar arasındakı məsafənin onların xətti ölçülərindən xeyli böyük olduğunu nəzərə alaraq təxmini hesablama aparmaq olar.
İkincisi, ideal qazdakı molekullar bir-biri ilə qarşılıqlı əlaqədə olmamalıdır. Əslində belə qarşılıqlı əlaqələr həmişə mövcuddur. Beləliklə, hətta nəcib qazların atomları da dipol-dipol cazibəsini yaşayır. Başqa sözlə, van der Waals qarşılıqlı əlaqəsi mövcuddur. Lakin molekulların fırlanma və translyasiya hərəkətinin kinetik enerjisi ilə müqayisədə bu qarşılıqlı təsirlər o qədər kiçikdir ki, qazların xassələrinə təsir göstərmir. Buna görə də praktiki məsələlərin həlli zamanı bunlar nəzərə alına bilməz.
Qeyd etmək lazımdır ki, sıxlığı aşağı və temperaturu yüksək olan bütün qazlar ideal hesab edilə bilməz. Van der Waals qarşılıqlı təsirlərinə əlavə olaraq, qazın ideallıq şərtlərinin kobud şəkildə pozulmasına səbəb olan H2O molekulları arasında hidrogen bağları kimi daha güclü bağ növləri də mövcuddur. Bu səbəbdən su buxarı ideal qaz deyil, hava idealdır.
İdeal qazın fiziki modeli
Bu modeli aşağıdakı kimi təqdim etmək olar: tutaq ki, qaz sistemində N hissəcik var. Bunlar müxtəlif kimyəvi maddələrin və elementlərin atomları və molekulları ola bilər. N hissəciklərin sayı böyükdür, ona görə də onu təsvir etmək üçün adətən “mol” vahidindən istifadə olunur (1 mol Avoqadro nömrəsinə uyğundur). Onların hamısı müəyyən həcmdə hərəkət edir V. Hissəciklərin hərəkətixaotik və bir-birindən müstəqildirlər. Onların hər birinin müəyyən v sürəti var və düz yolda hərəkət edir.
Nəzəri cəhətdən hissəciklər arasında toqquşma ehtimalı demək olar ki, sıfırdır, çünki onların ölçüləri hissəciklərarası məsafələrlə müqayisədə kiçikdir. Ancaq belə bir toqquşma baş verərsə, o, tamamilə elastikdir. Sonuncu halda, hissəciklərin ümumi impulsu və onların kinetik enerjisi saxlanılır.
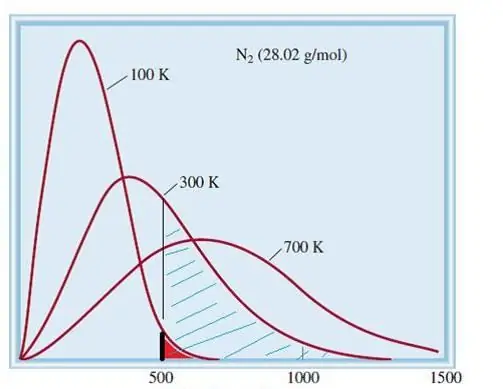
İdeal qazların nəzərdən keçirilən modeli çoxlu sayda elementə malik klassik sistemdir. Buna görə də onun tərkibindəki hissəciklərin sürəti və enerjisi Maksvell-Boltzmanın statistik paylanmasına tabedir. Bəzi hissəciklərin sürəti aşağı, bəzilərinin isə yüksək sürəti var. Bu vəziyyətdə, bu kəmiyyətin ən çox ehtimal olunan dəyərlərinin olduğu müəyyən bir dar sürət həddi var. Azot molekullarının sürət paylanması aşağıda sxematik şəkildə göstərilmişdir.
Qazların kinetik nəzəriyyəsi
Yuxarıda təsvir edilən ideal qazların modeli qazların xassələrini unikal şəkildə müəyyən edir. Bu model ilk dəfə 1738-ci ildə Daniel Bernoulli tərəfindən təklif edilmişdir.

Daha sonra Avqust Kroenig, Rudolf Clausius, Mixail Lomonosov, James Maxwell, Ludwig Boltzmann, Marian Smoluchowski və digər elm adamları tərəfindən indiki vəziyyətinə gətirildi.
İdeal qaz modelinin qurulduğu maye maddələrin kinetik nəzəriyyəsi mikroskopik davranışına əsaslanaraq sistemin iki mühüm makroskopik xassəsini izah edir:
- Qazlardakı təzyiq hissəciklərin qabın divarları ilə toqquşmasının nəticəsidir.
- Sistemdəki temperatur molekulların və atomların daimi hərəkətinin təzahürünün nəticəsidir.
Kinetik nəzəriyyənin hər iki nəticəsini genişləndirək.
Qaz təzyiqi
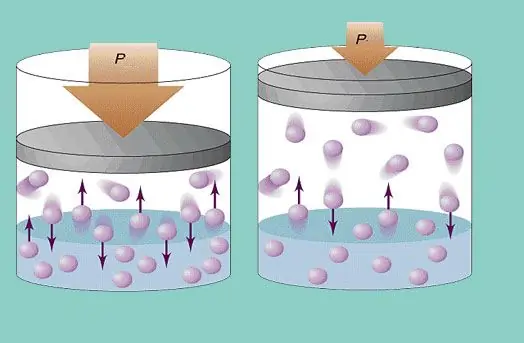
İdeal qaz modeli sistemdəki hissəciklərin daimi xaotik hərəkətini və onların damarın divarları ilə daimi toqquşmasını nəzərdə tutur. Hər bir belə toqquşma tamamilə elastik hesab olunur. Hissəcik kütləsi kiçikdir (≈10-27-10-25 kq). Buna görə də, toqquşma zamanı çox təzyiq yarada bilməz. Buna baxmayaraq, hissəciklərin sayı və deməli, toqquşmaların sayı çox böyükdür (≈1023). Bundan əlavə, elementlərin orta kvadrat sürəti otaq temperaturunda saniyədə bir neçə yüz metrdir. Bütün bunlar gəminin divarlarında nəzərəçarpacaq təzyiqin yaranmasına səbəb olur. Aşağıdakı düsturla hesablana bilər:
P=Nmvcp2 / (3V), burada vcp kök orta kvadrat sürət, m hissəcik kütləsidir.
Mütləq temperatur
İdeal qaz modelinə görə, temperatur öyrənilən sistemdəki molekul və ya atomun orta kinetik enerjisi ilə unikal şəkildə müəyyən edilir. İdeal qaz üçün kinetik enerji və mütləq temperaturu əlaqələndirən aşağıdakı ifadəni yaza bilərsiniz:
mvcp2 / 2=3 / 2kB T.
Burada kB Boltsman sabitidir. Bu bərabərlikdən əldə edirik:
T=m vcp2 / (3kB).
Universal vəziyyət tənliyi
Yuxarıdakı ifadələri mütləq təzyiq P və mütləq temperatur T üçün birləşdirsək, aşağıdakı bərabərliyi yaza bilərik:
PV=nRT.
Burada n maddənin mol ilə miqdarı, R D. İ. Mendeleyev tərəfindən verilmiş qaz sabitidir. Bu ifadə ideal qazlar nəzəriyyəsində ən mühüm tənlikdir, çünki o, üç termodinamik parametri (V, P, T) birləşdirir və qaz sisteminin kimyəvi xüsusiyyətlərindən asılı deyildir.

Universal tənlik ilk dəfə 19-cu əsrdə fransız fiziki Emil Klapeyron tərəfindən eksperimental olaraq əldə edilmiş və daha sonra rus kimyaçısı Mendeleyev tərəfindən müasir formasına gətirilmişdir və buna görə də hal-hazırda bu alimlərin adlarını daşıyır.






