Qazın istilik tutumu cismin bir dərəcə qızdırıldığı zaman qəbul etdiyi enerjinin miqdarıdır. Gəlin bu fiziki kəmiyyətin əsas xüsusiyyətlərini təhlil edək.

Təriflər
Qazın xüsusi istiliyi müəyyən bir maddənin vahid kütləsidir. Onun ölçü vahidləri J/(kg·K)-dir. Aqreqasiya vəziyyətinin dəyişməsi prosesində orqanizm tərəfindən qəbul edilən istilik miqdarı təkcə ilkin və son vəziyyətlə deyil, həm də keçid üsulu ilə əlaqələndirilir.

Departament
Qazların istilik tutumu sabit həcmdə (Cv), sabit təzyiqdə (Cр) müəyyən edilən qiymətə bölünür.
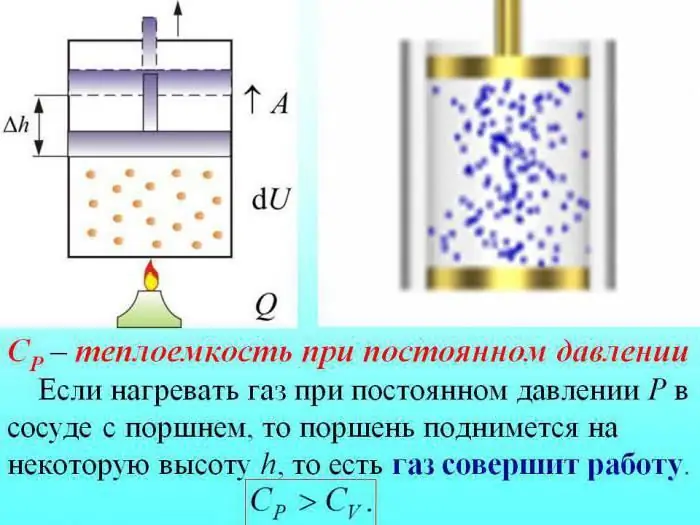
Təzyiq dəyişdirilmədən qızdırılma zamanı istiliyin bir hissəsi qazın genişlənməsi işinin istehsalına, enerjinin bir hissəsi isə daxili enerjinin artırılmasına sərf olunur.
Sabit təzyiqdə qazların istilik tutumu daxili enerjinin artırılmasına sərf olunan istilik miqdarı ilə müəyyən edilir.
Qaz vəziyyəti: xüsusiyyətlər, təsvir
İdeal qazın istilik tutumu Сp-Сv=R nəzərə alınmaqla müəyyən edilir. Sonuncu kəmiyyət universal qaz sabiti adlanır. Onun dəyəri 8,314 J/(mol K) uyğundur.
İstilik tutumunun nəzəri hesablamalarını apararkən, məsələn, temperaturla əlaqəni təsvir edərkən təkcə termodinamik metodlardan istifadə etmək kifayət deyil, statik fizikanın elementləri ilə silahlanmaq vacibdir.
Qazların istilik tutumu bəzi molekulların ötürmə hərəkətinin enerjisinin orta qiymətinin hesablanmasını nəzərdə tutur. Belə hərəkət molekulun fırlanma və köçürmə hərəkətindən, həmçinin atomların daxili titrəyişlərindən ümumiləşdirilmişdir.
Statik fizikada fırlanma və ötürmə hərəkətinin hər bir azadlığı dərəcəsi üçün universal qaz sabitinin yarısına bərabər olan bir qazın kəmiyyəti olduğu barədə məlumat var.

Maraqlı faktlar
Monatomik qazın zərrəciyinin üç tərcümə sərbəstlik dərəcəsi olduğu qəbul edilir, ona görə də qazın xüsusi istiliyinin üç ötürmə, iki fırlanma və bir vibrasiya sərbəstlik dərəcəsi vardır. Onların vahid paylanması qanunu sabit həcmdə xüsusi istiliyi R-ə bərabərləşdirməyə gətirib çıxarır.
Təcrübələr zamanı müəyyən edilmişdir ki, iki atomlu qazın istilik tutumu R qiymətinə uyğundur. Nəzəriyyə ilə praktika arasındakı bu cür uyğunsuzluq, ideal qazın istilik tutumunun kvantla bağlı olması ilə izah olunur. təsirlər, buna görə də hesablamalar apararkən, kvant əsasında statistikadan istifadə etmək vacibdirmexanika.
Kvant mexanikasının əsaslarına əsasən, qaz molekulları da daxil olmaqla salınan və ya fırlanan istənilən hissəciklər sistemi yalnız bəzi diskret enerji dəyərlərinə malikdir.
Sistemdəki istilik hərəkətinin enerjisi müəyyən tezlikli salınımları həyəcanlandırmaq üçün kifayət deyilsə, belə hərəkətlər sistemin ümumi istilik tutumuna töhfə vermir.
Nəticədə müəyyən bir azadlıq dərəcəsi "donmuş" olur, ona bərabər bölgü qanununu tətbiq etmək mümkün deyil.
Qazların istilik tutumu bütün termodinamik sistemin işləməsinin asılı olduğu vəziyyətin mühüm xarakteristikasıdır.
Evibrasiya və ya fırlanma sərbəstlik dərəcəsinə bərabər bölünmə qanununun tətbiq oluna biləcəyi temperatur kvant nəzəriyyəsi ilə xarakterizə olunur, Plank sabitini Boltsman sabiti ilə əlaqələndirir.

Diatomik qazlar
Belə qazların fırlanma enerji səviyyələri arasındakı boşluqlar az sayda dərəcədir. İstisna hidrogendir, burada temperatur dəyəri yüzlərlə dərəcə ilə müəyyən edilir.
Ona görə də sabit təzyiqdə qazın istilik tutumunu vahid paylanma qanunu ilə təsvir etmək çətindir. Kvant statistikasında istilik tutumu müəyyən edilərkən nəzərə alınır ki, onun vibrasiya hissəsi temperaturun aşağı düşməsi zamanı tez azalır və sıfıra çatır.
Bu fenomen otaq temperaturunda istilik tutumunun praktiki olaraq heç bir vibrasiya hissəsinin olmaması faktını izah edir.iki atomlu qaz, sabit R-ə uyğundur.
Aşağı temperatur göstəriciləri zamanı sabit həcmdə qazın istilik tutumu kvant statistikasından istifadə etməklə müəyyən edilir. Termodinamikanın üçüncü qanunu adlanan Nernst prinsipi var. Tərkibinə əsasən, qazın molar istilik tutumu temperaturun azalması ilə sıfıra doğru azalacaq.

Bərk maddələrin xüsusiyyətləri
Qazların qarışığının istilik tutumunu kvant statistikası ilə izah etmək olarsa, bərk birləşmə vəziyyəti üçün istilik hərəkəti tarazlıq vəziyyətinə yaxın hissəciklərin cüzi dalğalanmaları ilə xarakterizə olunur.
Hər atomun üç vibrasiya sərbəstlik dərəcəsi var, buna görə də, bərabər bölmə qanununa uyğun olaraq, bərk cismin molar istilik tutumu 3nR kimi hesablana bilər, n isə molekuldakı atomların sayıdır.
Təcrübədə bu rəqəm bərk cismin istilik tutumunun yüksək temperaturda meyl etdiyi hədddir.
Bəzi elementlər, o cümlədən metallar üçün adi temperaturda maksimum əldə etmək olar. n=1 üçün Dulong və Petit qanunu yerinə yetirilir, lakin mürəkkəb maddələr üçün belə bir həddə çatmaq olduqca çətindir. Reallıqda həddi əldə etmək mümkün olmadığı üçün bərk maddənin parçalanması və ya əriməsi baş verir.
Kvant nəzəriyyəsinin tarixi
Kvant nəzəriyyəsinin yaradıcıları iyirminci əsrin əvvəllərində Eynşteyn və Debaydır. Müəyyən bir yerdə atomların salınım hərəkətlərinin kvantlaşdırılmasına əsaslanırkristal. Aşağı temperatur göstəriciləri vəziyyətində, bərk cismin istilik tutumu kub şəklində alınan mütləq dəyərlə birbaşa mütənasib olur. Bu əlaqə Debye qanunu adlanır. Aşağı və yüksək temperatur göstəricilərini ayırd etməyə imkan verən meyar kimi onların Debye temperaturu ilə müqayisəsi götürülür.
Bu dəyər bədəndəki atomun titrəyişlərinin spektri ilə müəyyən edilir, buna görə də onun kristal quruluşunun xüsusiyyətlərindən ciddi şəkildə asılıdır.
QD bir neçə yüz K olan dəyərdir, lakin, məsələn, almazda daha yüksəkdir.
Keçirici elektronlar metalların istilik tutumuna əhəmiyyətli töhfə verir. Bunu hesablamaq üçün Fermi kvant statistikasından istifadə olunur. Metal atomları üçün elektron keçiricilik mütləq temperaturla düz mütənasibdir. Əhəmiyyətsiz dəyər olduğu üçün yalnız mütləq sıfıra meylli temperaturlarda nəzərə alınır.
İstilik tutumunun təyini üsulları
Əsas eksperimental üsul kalorimetriyadır. İstilik tutumunun nəzəri hesabını aparmaq üçün statistik termodinamikadan istifadə olunur. İdeal qaz üçün, eləcə də kristal cisimlər üçün keçərlidir, maddənin quruluşuna dair eksperimental məlumatlar əsasında aparılır.
İdeal qazın istilik tutumunun hesablanması üçün empirik üsullar kimyəvi quruluş ideyasına, ayrı-ayrı atom qruplarının Ср-a verdiyi töhfəyə əsaslanır.
Mayelər üçün termodinamikadan istifadəyə əsaslanan üsullardan da istifadə olunurbuxarlanma prosesinin entalpiyasının temperaturunun törəməsi vasitəsilə ideal qazın istilik tutumundan mayeyə keçməyi mümkün edən dövrlər.
Məhl halında istilik tutumunun əlavə funksiya kimi hesablanmasına icazə verilmir, çünki məhlulun istilik tutumunun artıq dəyəri əsasən əhəmiyyətlidir.
Bunu qiymətləndirmək üçün bizə məhlulların molekulyar-statistik nəzəriyyəsi lazımdır. Ən çətini termodinamik analizdə heterojen sistemlərin istilik tutumunun müəyyən edilməsidir.

Nəticə
İstilik tutumunun öyrənilməsi kimyəvi reaktorlarda, eləcə də digər kimyəvi istehsal aparatlarında baş verən proseslərin enerji balansını hesablamağa imkan verir. Bundan əlavə, bu dəyər optimal soyuducu növlərinin seçilməsi üçün lazımdır.
Hazırda maddələrin istilik tutumunun müxtəlif temperatur intervalları üçün - aşağı qiymətlərdən yüksək dəyərlərə qədər - eksperimental təyini bir maddənin termodinamik xüsusiyyətlərini təyin etmək üçün əsas seçimdir. Maddənin entropiyasını və entalpiyasını hesablayarkən istilik tutumunun inteqrallarından istifadə olunur. Müəyyən bir temperatur diapazonunda kimyəvi reagentlərin istilik tutumu haqqında məlumat prosesin istilik effektini hesablamağa imkan verir. Məhlulların istilik tutumu haqqında məlumat onların termodinamik parametrlərini təhlil edilən intervalda istənilən temperatur dəyərlərində hesablamağa imkan verir.
Məsələn, maye potensial enerjinin dəyərini dəyişmək üçün istiliyin bir hissəsinin xərclənməsi ilə xarakterizə olunur.reaksiya verən molekullar. Bu dəyər həlləri təsvir etmək üçün istifadə edilən "konfiqurasiya" istilik tutumu adlanır.
Maddənin termodinamik xüsusiyyətlərini, onun birləşmə vəziyyətini nəzərə almadan tam riyazi hesablamalar aparmaq çətindir. Məhz buna görə də mayelər, qazlar, bərk cisimlər üçün maddənin enerji parametrlərini xarakterizə etməyə imkan verən xüsusi istilik tutumu kimi bir xüsusiyyət istifadə olunur.






