İdeal qaz, ideal qaz hal tənliyi, onun temperaturu və təzyiqi, həcmi… fizikanın müvafiq bölməsində istifadə olunan parametr və təriflərin siyahısını kifayət qədər uzun müddət davam etdirmək olar. Bu gün biz yalnız bu mövzuda danışacağıq.
Molekulyar fizikada nə nəzərdə tutulur?

Bu bölmədə nəzərdən keçirilən əsas obyekt ideal qazdır. İdeal qaz vəziyyəti tənliyi normal ekoloji şərait nəzərə alınmaqla əldə edilmişdir və bu barədə bir az sonra danışacağıq. İndi gəlin bu "problemə" uzaqdan yanaşaq.
Tutaq ki, bizdə qaz kütləsi var. Onun vəziyyəti termodinamik xarakterli üç parametrdən istifadə etməklə müəyyən edilə bilər. Bunlar təbii ki, təzyiq, həcm və temperaturdur. Bu vəziyyətdə sistemin vəziyyətinin tənliyi müvafiq parametrlər arasındakı əlaqə üçün düstur olacaqdır. Bu belə görünür: F (p, V, T)=0.
Burada ilk dəfə olaraq ideal kimi bir şeyin ortaya çıxmasına yavaş-yavaş yaxınlaşırıq.qaz. Molekullar arasında qarşılıqlı təsirlərin əhəmiyyətsiz olduğu qaz adlanır. Ümumiyyətlə, təbiətdə bu yoxdur. Bununla belə, istənilən yüksək dərəcədə nadirləşdirilmiş qaz ona yaxındır. Normal şəraitdə olan azot, oksigen və hava idealdan az fərqlənir. İdeal qazın vəziyyət tənliyini yazmaq üçün vahid qaz qanunundan istifadə edə bilərik. Alırıq: pV/T=const.
Əlaqədar Konsepsiya №1: Avoqadro Qanunu
O, bizə deyə bilər ki, əgər biz tamamilə hər hansı təsadüfi qazın eyni sayda molunu götürsək və onları temperatur və təzyiq daxil olmaqla, eyni şərtlərə qoysaq, qazlar eyni həcmdə olacaq. Xüsusilə, təcrübə normal şəraitdə aparılıb. Bu o deməkdir ki, temperatur 273,15 Kelvin, təzyiq bir atmosfer (760 millimetr civə və ya 101325 Paskal) idi. Bu parametrlərlə qaz 22,4 litrə bərabər bir həcm tutdu. Buna görə də deyə bilərik ki, hər hansı bir qazın bir mol üçün ədədi parametrlərin nisbəti sabit bir dəyər olacaqdır. Buna görə də bu rəqəmi R hərfi ilə təyin etmək və onu universal qaz sabiti adlandırmaq qərara alındı. Beləliklə, o, 8.31-ə bərabərdir. Vahid J/molK-dır.
İdeal qaz. Vəziyyətin ideal qaz tənliyi və onun manipulyasiyası
Düsulu yenidən yazmağa çalışaq. Bunun üçün onu bu formada yazırıq: pV=RT. Sonra, sadə bir hərəkət edirik, tənliyin hər iki tərəfini ixtiyari sayda mol ilə çarpırıq. Biz pVu=uRT alırıq. Nəzərə alaq ki, molar həcminin hasili vəmaddənin miqdarı sadəcə həcmdir. Ancaq bütün bunlardan sonra molların sayı eyni vaxtda kütlənin və molyar kütlənin nisbətinə bərabər olacaqdır. Mendeleyev-Klapeyron tənliyi məhz belə görünür. İdeal qazın hansı sistemdən ibarət olduğu barədə aydın təsəvvür yaradır. İdeal qaz üçün vəziyyət tənliyi aşağıdakı formanı alacaq: pV=mRT/M.
Təzyiq düsturu çıxarın
Alınan ifadələrlə daha bir neçə manipulyasiya edək. Bunun üçün Mendeleyev-Klapeyron tənliyinin sağ tərəfi Avoqadro ədədinə vurulur və bölünür. İndi Avogadro nömrəsi ilə maddə miqdarının məhsuluna diqqətlə baxırıq. Bu qazdakı molekulların ümumi sayından başqa bir şey deyil. Lakin eyni zamanda universal qaz sabitinin Avoqadro ədədinə nisbəti Boltzman sabitinə bərabər olacaqdır. Buna görə də təzyiq üçün düsturlar aşağıdakı kimi yazıla bilər: p=NkT/V və ya p=nkT. Burada n simvolu hissəcik konsentrasiyasıdır.
İdeal qaz prosesləri
Molekulyar fizikada izoproseslər kimi bir şey var. Bunlar sistemdə sabit parametrlərdən birində baş verən termodinamik proseslərdir. Bu zaman maddənin kütləsi də sabit qalmalıdır. Onlara daha konkret baxaq. Beləliklə, ideal qazın qanunları.
Təzyiq sabit qalır
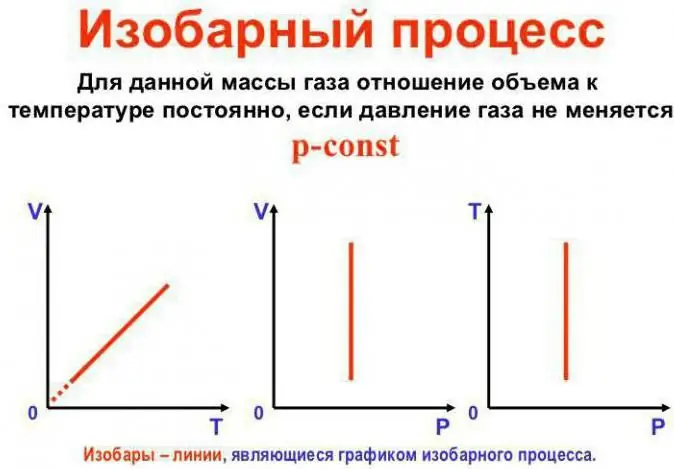
Bu, Gay-Lussac qanunudur. Bu belə görünür: V/T=const. Başqa bir şəkildə yenidən yazmaq olar: V=Vo (1 + at). Burada a 1/273,15 K^-1-ə bərabərdir və “həcm genişlənmə əmsalı” adlanır. Həm Selsi, həm də temperaturu əvəz edə bilərikKelvin şkalası. Sonuncu halda V=Voat düsturu alırıq.
Səs sabit qalır

Bu, Gay-Lussacın ikinci qanunudur, daha çox Çarlz qanunu kimi istinad edilir. Bu belə görünür: p/T=const. Başqa bir formula var: p=po (1 + at). Transformasiyalar əvvəlki nümunəyə uyğun olaraq həyata keçirilə bilər. Gördüyünüz kimi, ideal qaz qanunları bəzən bir-birinə tamamilə bənzəyir.
Temperatur sabit qalır

İdeal qazın temperaturu sabit qalsa, Boyl-Mariot qanununu əldə edə bilərik. Bunu belə yazmaq olar: pV=const.
Əlaqədar Konsepsiya №2: Qismən Təzyiq
Deyək ki, qazları olan bir gəmimiz var. Qarışıq olacaq. Sistem istilik tarazlığı vəziyyətindədir və qazların özləri bir-biri ilə reaksiya vermir. Burada N molekulların ümumi sayını göstərəcək. N1, N2 və s., müvafiq olaraq, qarışığın komponentlərinin hər birindəki molekulların sayı. P=nkT=NkT/V təzyiq düsturunu götürək. Müəyyən bir iş üçün açıla bilər. İki komponentli qarışıq üçün formula aşağıdakı formanı alacaq: p=(N1 + N2) kT/V. Ancaq sonra məlum olur ki, ümumi təzyiq hər qarışığın qismən təzyiqlərindən cəmlənəcəkdir. Beləliklə, p1 + p2 və s. kimi görünəcək. Bunlar qismən təzyiqlər olacaq.
Nə üçündür?
Əldə etdiyimiz düstur sistemdəki təzyiqin hər molekul qrupundan olduğunu göstərir. Yeri gəlmişkən, ondan asılı deyilbaşqaları. D alton qanunu tərtib edərkən bundan istifadə etdi və sonradan onun adını daşıdı: qazların bir-biri ilə kimyəvi reaksiya vermədiyi qarışıqda ümumi təzyiq qismən təzyiqlərin cəminə bərabər olacaq.






