Maye suyun üçölçülü vəziyyətini öyrənmək çətindir, lakin buz kristallarının strukturunu təhlil etməklə çox şey öyrənilib. Dörd qonşu hidrogenlə qarşılıqlı təsir göstərən oksigen atomu tetraedrin təpələrini tutur (tetra=dörd, hedron=müstəvi). Buzda belə bir bağı qırmaq üçün tələb olunan orta enerji 23 kJ/mol-1 hesablanır.

Su molekullarının müəyyən sayda hidrogen zəncirləri yaratmaq qabiliyyəti, eləcə də verilən güc qeyri-adi yüksək ərimə nöqtəsi yaradır. Əridikdə, quruluşu nizamsız olan maye su ilə tutulur. Hidrogen bağlarının çoxu pozulur. Hidrogenlə bağlanmış buzun kristal qəfəsini parçalamaq üçün istilik şəklində böyük miqdarda enerji tələb olunur.
Buzun görünüşünün xüsusiyyətləri (Ih)
Sakinlərin çoxu buzun hansı kristal qəfəsə malik olduğu ilə maraqlanır. ZəruriQeyd etmək lazımdır ki, əksər maddələrin sıxlığı dondurma zamanı, molekulyar hərəkətlər ləngidikdə və sıx yığılmış kristallar əmələ gələndə artır. Suyun sıxlığı da maksimum 4°C-də (277K) soyuduqca artır. Sonra temperatur bu dəyərdən aşağı düşəndə genişlənir.
Bu artım, hər bir su molekulunun yuxarıdakı element və dörd digər dəyərlə sərt şəkildə bağlandığı, qəfəsli və daha aşağı sıxlığı olan, açıq, hidrogen bağlı buz kristalının əmələ gəlməsi ilə əlaqədardır. daha çox kütlə var. Bu hərəkət baş verdiyi üçün maye yuxarıdan aşağıya doğru donur. Bunun mühüm bioloji nəticələri var, nəticədə gölməçədəki buz təbəqəsi canlıları həddindən artıq soyuqdan izolyasiya edir. Bundan əlavə, suyun iki əlavə xüsusiyyəti onun hidrogen xüsusiyyətləri ilə bağlıdır: xüsusi istilik və buxarlanma.
Strukturların ətraflı təsviri
Birinci meyar maddənin 1 qramının temperaturunu 1°C yüksəltmək üçün lazım olan miqdardır. Suyun dərəcələrini yüksəltmək nisbətən böyük miqdarda istilik tələb edir, çünki hər bir molekul kinetik enerjinin artması üçün qırılmalı olan çoxsaylı hidrogen bağlarında iştirak edir. Yeri gəlmişkən, bütün böyük çoxhüceyrəli orqanizmlərin hüceyrə və toxumalarında H2O-nun çoxluğu hüceyrələrin daxilində temperaturun dəyişməsinin minimuma endirilməsi deməkdir. Bu xüsusiyyət çox vacibdir, çünki əksər biokimyəvi reaksiyaların sürətihəssas.
Suyun buxarlanma istiliyi də bir çox digər mayelərdən xeyli yüksəkdir. Bu cismi qaza çevirmək üçün böyük miqdarda istilik lazımdır, çünki su molekullarının bir-birindən ayrılaraq sözügedən faza daxil olması üçün hidrogen bağlarının qırılması lazımdır. Dəyişən cisimlər daimi dipollardır və digər oxşar birləşmələrlə və ionlaşdıran və həll olunanlarla qarşılıqlı əlaqədə ola bilər.
Yuxarıda qeyd olunan digər maddələr yalnız polarite olduqda təmasda ola bilər. Bu elementlərin strukturunda iştirak edən bu birləşmədir. Bundan əlavə, o, elektrolitlərdən əmələ gələn bu hissəciklərin ətrafında düzləşə bilər ki, su molekullarının mənfi oksigen atomları kationlara, müsbət ionlar və hidrogen atomları isə anionlara yönəlsin.
Bərk cisimlərdə, bir qayda olaraq, molekulyar kristal qəfəslər və atomik olanlar əmələ gəlir. Yəni, yod elə qurulubsa ki, tərkibində I2, , bərk karbon qazında, yəni quru buzda CO2 molekulları olur. kristal qəfəs qovşaqlarında yerləşir . Bənzər maddələrlə qarşılıqlı əlaqədə olduqda, buz ion kristal şəbəkəsinə malikdir. Məsələn, karbon əsasında atom quruluşuna malik olan qrafit, almaz kimi onu dəyişdirə bilmir.
Xörək duzunun kristalı suda həll edildikdə nə baş verir: qütb molekulları kristaldakı yüklü elementlərə cəlb olunur, bu da onun səthində oxşar natrium və xlorid hissəciklərinin əmələ gəlməsinə səbəb olur və nəticədə bu cisimlər yaranır.bir-birindən ayrılır və əriməyə başlayır. Buradan buzun ion əlaqəsi olan kristal qəfəsə malik olduğunu müşahidə etmək olar. Hər həll olunmuş Na + bir neçə su molekulunun mənfi uclarını, hər həll olunmuş Cl isə müsbət uclarını çəkir. Hər bir ionu əhatə edən qabıq qaçış sferası adlanır və adətən bir neçə qat həlledici hissəciklərdən ibarətdir.
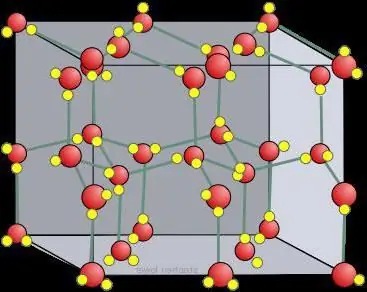
Quru buz kristal şəbəkəsi
Dəyişənlər və ya elementlərlə əhatə olunmuş ion sulfatlanmış deyilir. Həlledici su olduqda, belə hissəciklər nəmlənir. Beləliklə, hər hansı bir qütb molekulu maye cismin elementləri tərəfindən həll olunmağa meyllidir. Quru buzda kristal qəfəs növü aqreqasiya vəziyyətində dəyişməz olan atom bağları əmələ gətirir. Başqa bir şey kristal buzdur (donmuş su). Karboksilaza və protonlanmış aminlər kimi ion üzvi birləşmələr hidroksil və karbonil qruplarında həll olmalıdır. Belə strukturlarda olan hissəciklər molekullar arasında hərəkət edir və onların qütb sistemləri bu bədənlə hidrogen bağları yaradır.
Əlbəttə, molekulda sonuncu göstərilən qrupların sayı onun həll olunma qabiliyyətinə təsir edir, bu da elementdəki müxtəlif strukturların reaksiyasından asılıdır: məsələn, bir, iki və üç karbonlu spirtlər qarışdırılır. su ilə, lakin tək hidroksil birləşmələri olan daha böyük karbohidrogenlər mayelərdə daha az seyreltilir.
Altıbucaqlı Ih formasına bənzəyiratom kristal qəfəsi. Buz və Yerdəki bütün təbii qarlar üçün bu, tam olaraq belə görünür. Bunu su buxarından (yəni qar dənəcikləri) böyüdülmüş buz kristal şəbəkəsinin simmetriyası sübut edir. 194-dən P 63/mm kosmik qrupundadır; D 6h, Laue sinfi 6/mm; 6 spiral oxunun qatına malik olan β- kimi (onun boyunca yerdəyişməyə əlavə olaraq ətrafında fırlanma). Sadə kub (~1/2) və ya üz mərkəzli kub (~3/4) strukturlarla müqayisədə səmərəliliyin aşağı olduğu (~1/3) kifayət qədər açıq aşağı sıxlıqlı struktura malikdir.
Adi buzla müqayisədə CO2 molekulları ilə bağlanmış quru buzun kristal qəfəsi statikdir və yalnız atomlar parçalandıqda dəyişir.
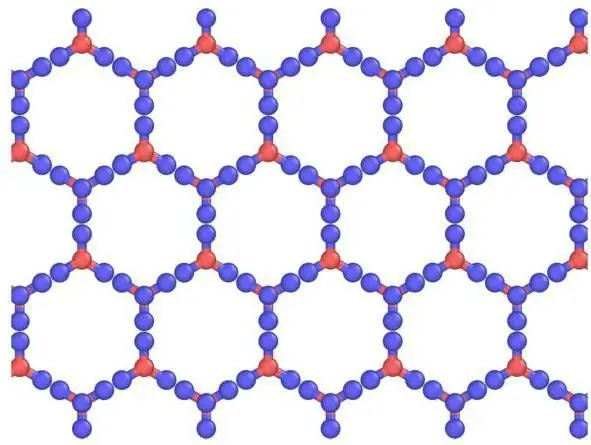
Qarışların və onların elementlərinin təsviri
Kristallara bir-birinin üstünə qoyulmuş təbəqələrdən ibarət kristal modellər kimi baxmaq olar. Hidrogen bağı sifarişlidir, əslində isə təsadüfi olur, çünki protonlar təxminən 5 K-dən yuxarı temperaturda su (buz) molekulları arasında hərəkət edə bilirlər. Həqiqətən də, çox güman ki, protonlar daimi tunel axınında kvant mayesi kimi davranırlar. Bu, neytronların səpilməsi ilə gücləndirilir, onların səpilmə sıxlığını oksigen atomları arasında yarıya qədər göstərir, lokalizasiyanı və uyğunlaşdırılmış hərəkəti göstərir. Burada buzun atomik, molekulyar kristal qəfəslə oxşarlığı var.
Molekullar hidrogen zəncirinin pilləli düzülüşünə malikdirtəyyarədəki üç qonşusuna münasibətdə. Dördüncü elementin tutulmuş hidrogen bağı təşkili var. Mükəmməl altıbucaqlı simmetriyadan cüzi bir sapma var, çünki vahid hüceyrə bu zəncirin istiqamətində 0,3% qısadır. Bütün molekullar eyni molekulyar mühiti yaşayır. Hər bir "qutu" içərisində interstisial suyun hissəciklərini saxlamaq üçün kifayət qədər yer var. Ümumiyyətlə nəzərə alınmasa da, onlar bu yaxınlarda buzun toz kristal qəfəsinin neytron difraksiyası ilə effektiv şəkildə aşkar edilmişdir.
Dəyişən Maddələr
Altıbucaqlı gövdə maye və qazlı su 0,01 ° C, 612 Pa, bərk elementlər ilə üçlü nöqtələrə malikdir - üç -21,985 ° C, 209,9 MPa, on bir və iki -199,8 ° C, 70 MPa, eləcə də - 34,7 ° C, 212,9 MPa. Altıbucaqlı buzun dielektrik davamlılığı 97,5-dir.
Bu elementin ərimə əyrisi MPa ilə verilir. Vəziyyət tənlikləri, onlara əlavə olaraq, altıbucaqlı buzun və onun sulu süspansiyonlarının temperaturu ilə fiziki xassələrin dəyişməsi ilə əlaqəli bəzi sadə bərabərsizliklər mövcuddur. Sərtlik, 0°C-də gipsdən (≦2) aşağı və ya -80°C-də feldispata (6 Mohs) qədər yüksələn dərəcələrlə dəyişir, mütləq sərtlikdə qeyri-adi dərəcədə böyük dəyişiklik (> 24 dəfə).
Buzun altıbucaqlı kristal qəfəsi altıbucaqlı lövhələr və sütunlar əmələ gətirir, burada yuxarı və aşağı üzlər 5,57 μJ sm entalpiyası olan bazal müstəvilərdir {0 0 0 1} -2və digər ekvivalent yan hissələrə 5, 94 olan {1 0 -1 0} prizmasının hissələri deyilir.µJ cm -2. 6,90 ΜJ ˣ sm -2 olan ikinci dərəcəli səthlər {1 1 -2 0} konstruksiyaların yan tərəflərinin yaratdığı müstəvilər boyunca formalaşa bilər.
Belə bir quruluş artan təzyiqlə istilik keçiriciliyində anomal azalma göstərir (həmçinin aşağı sıxlıqlı kub və amorf buz), lakin əksər kristallardan fərqlənir. Bu, buz və suyun kristal qəfəsindəki səsin eninə sürətini azaldan hidrogen bağının dəyişməsi ilə bağlıdır.
Böyük kristal nümunələrinin və istənilən buz səthinin necə hazırlanacağını təsvir edən üsullar var. Tədqiq olunan altıbucaqlı cismin səthindəki hidrogen bağının toplu sistemin daxilində olduğundan daha nizamlı olacağı güman edilir. Faza-torlu tezlik generasiyası ilə variasiya spektroskopiyası altıbucaqlı buzun bazal səthinin yer altı H2O zəncirində iki yuxarı təbəqə (L1 və L2) arasında struktur asimmetriyasının olduğunu göstərdi. Altıbucaqlıların yuxarı təbəqələrində qəbul edilmiş hidrogen bağları (L1 O ··· HO L2) ikinci təbəqədə yuxarı yığılmaya (L1 OH ··· O L2) qəbul edilənlərdən daha güclüdür. İnteraktiv altıbucaqlı buz konstruksiyaları mövcuddur.
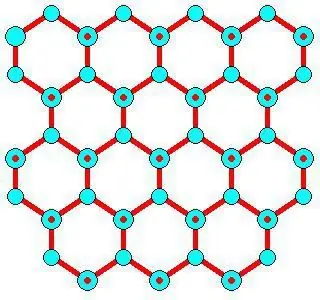
İnkişaf Xüsusiyyətləri
Buz əmələ gətirmək üçün lazım olan minimum su molekullarının sayı 280-dən ibarət tam ikosahedral çoxluqda olduğu kimi təxminən 275 ± 25-dir. Yarama 10 10 sürətlə baş verir. hava-su interfeysi və toplu suda deyil. Buz kristallarının böyüməsi müxtəlif böyümə sürətlərindən asılıdırenerjilər. Bioloji nümunələr, qida və orqanların dondurulması zamanı su donmaqdan qorunmalıdır.
Bu, adətən, sürətli soyutma dərəcələri, kiçik nümunələr və kriokonservatordan istifadə etməklə və buzu nüvələşdirmək və hüceyrə zədələnməsinin qarşısını almaq üçün təzyiqi artırmaqla əldə edilir. Buz/mayenin sərbəst enerjisi atmosfer təzyiqində ~30 mJ/m2-dən 200 MPa-da 40 mJ/m-2-ə qədər artır. bu təsirin baş vermə səbəbi.
Buz üçün hansı növ kristal qəfəs xarakterikdir
Alternativ olaraq, onlar prizma səthlərindən (S2), tez donmuş və ya həyəcanlanmış göllərin təsadüfi pozulmuş səthində daha sürətli böyüyə bilərlər. {1 1 -2 0} üzlərindən böyümə ən azı eynidir, lakin onları prizma əsaslarına çevirir. Buz kristalının inkişafı ilə bağlı məlumatlar tam şəkildə araşdırılıb. Müxtəlif üzlərin elementlərinin nisbi artım templəri böyük dərəcədə birgə nəmləndirmə yaratmaq qabiliyyətindən asılıdır. Ətrafdakı suyun temperaturu (aşağı) buz kristalında budaqlanma dərəcəsini müəyyən edir. Hissəciklərin böyüməsi aşağı dərəcədə supersoyutmada, yəni <2 °C-də diffuziya sürəti ilə məhdudlaşır, nəticədə onların daha çox olur.

Ancaq >4°C yüksək depressiya səviyyələrində inkişaf kinetikası ilə məhdudlaşır, nəticədə iynə böyüməsi ilə nəticələnir. Bu forma quru buzun quruluşuna bənzəyir (altıbucaqlı quruluşa malik kristal qəfəsə malikdir), müxtəlifsəthin inkişafının xüsusiyyətləri və qar dənəciklərinin düz formalarının arxasında olan ətrafdakı (supersoyudulmuş) suyun temperaturu.
Atmosferdə buzun əmələ gəlməsi buludların əmələ gəlməsinə və xassələrinə dərindən təsir edir. Hər il milyonlarla ton atmosferə daxil olan səhra tozunda tapılan feldispatlar mühüm əmələ gələnlərdir. Kompüter simulyasiyaları göstərdi ki, bu, yüksək enerjili səth müstəvilərində prizmatik buz kristal müstəvilərinin nüvələşməsi ilə bağlıdır.
Bəzi digər elementlər və qəfəslər
Həll edilmiş maddələr (aralıqlara daxil ola bilən çox kiçik helium və hidrogen istisna olmaqla) atmosfer təzyiqində Ih strukturuna daxil edilə bilməz, lakin onların hissəcikləri arasında səthə və ya amorf təbəqəyə zorla çıxarılır. mikrokristal bədən. Quru buzun qəfəs yerlərində bəzi başqa elementlər də var: NH4 + və Cl - kimi xaotrop ionlar Na + və SO42-kimi digər kosmotropiklərə nisbətən daha yüngül maye dondurulmasına daxil olan, buna görə də kristallar arasında qalan mayenin nazik bir təbəqəsini meydana gətirdikləri üçün onları çıxarmaq mümkün deyil. Bu, qalan yükləri tarazlayan səth suyunun dissosiasiyası (bu, həmçinin maqnit şüalanmasına səbəb ola bilər) və qalıq maye filmlərin pH-nın dəyişməsi, məsələn, NH 4 səbəbiylə səthin elektrik yüklənməsinə səbəb ola bilər.2SO4 daha turşulu olur və NaCl daha əsas olur.
Onlar üzlərə perpendikulyardırəlavə edilmiş növbəti təbəqəni göstərən buzun kristal qəfəsi (qara rəngdə O atomları ilə). Onlar yavaş-yavaş böyüyən bazal səth {0 0 0 1} ilə xarakterizə olunur, burada yalnız təcrid olunmuş su molekulları birləşir. Prizmanın sürətlə böyüyən {1 0 -1 0} səthi, burada yeni birləşmiş hissəciklər cütləri bir-biri ilə hidrogenlə bağlana bilər (bir hidrogen bağı/elementin iki molekulu). Ən sürətlə böyüyən üz {1 1 -2 0} (ikinci dərəcəli prizmatik) dir, burada yeni birləşən hissəciklərin zəncirləri hidrogen bağı ilə bir-biri ilə qarşılıqlı əlaqədə ola bilər. Onun zəncirlərindən/element molekullarından biri bölən və prizmanın iki tərəfinə çevrilməni təşviq edən silsilələr əmələ gətirən formadır.
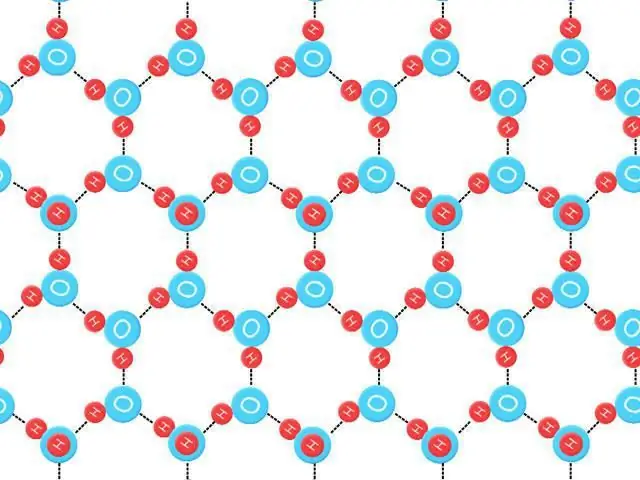
Sıfır nöqtəli entropiya
S 0=k B ˣ Ln (N E0) kimi təyin edilə bilər burada k B Boltzman sabitidir, NE E enerjisindəki konfiqurasiyaların sayı, E0 isə ən aşağı enerjidir. Sıfır Kelvində altıbucaqlı buzun entropiyası üçün bu dəyər termodinamikanın üçüncü qanununu pozmur "Mütləq sıfırda ideal kristalın entropiyası tam olaraq sıfırdır" çünki bu elementlər və hissəciklər ideal deyil, nizamsız hidrogen bağına malikdir.
Bu bədəndə hidrogen bağı təsadüfi və sürətlə dəyişir. Bu strukturlar enerji baxımından tam bərabər deyil, lakin çox sayda enerji baxımından yaxın vəziyyətlərə yayılır, "buz qaydalarına" tabe olur. Sıfır nöqtəli entropiya, material mütləq soyudulsa belə qalacaq pozğunluqdursıfır (0 K=-273, 15 ° C). Altıbucaqlı buz 3, 41 (± 0, 2) ˣ mol -1 ˣ K -1 üçün eksperimental qarışıqlıq yaradır. Nəzəri olaraq, məlum buz kristallarının sıfır entropiyasını eksperimental olaraq müəyyən etməkdən daha çox dəqiqliklə (qüsurları və enerji səviyyəsinin yayılmasını nəzərə almadan) hesablamaq mümkün olardı.
Alimlər və onların bu sahədəki işləri
S 0=k B ˣ Ln (N E0) kimi təyin edilə bilər burada k B Boltzman sabitidir, NE E enerjisindəki konfiqurasiyaların sayı, E0 isə ən aşağı enerjidir. Sıfır Kelvində altıbucaqlı buzun entropiyası üçün bu dəyər termodinamikanın üçüncü qanununu pozmur "Mütləq sıfırda ideal kristalın entropiyası tam olaraq sıfırdır" çünki bu elementlər və hissəciklər ideal deyil, nizamsız hidrogen bağına malikdir.
Bu bədəndə hidrogen bağı təsadüfi və sürətlə dəyişir. Bu strukturlar enerji baxımından tam bərabər deyil, lakin çox sayda enerji baxımından yaxın vəziyyətlərə yayılır, "buz qaydalarına" tabe olur. Sıfır nöqtəli entropiya, material mütləq sıfıra (0 K=-273.15 ° C) qədər soyudulsa belə qalacaq pozğunluqdur. Altıbucaqlı buz 3, 41 (± 0, 2) ˣ mol -1 ˣ K -1 üçün eksperimental qarışıqlıq yaradır. Nəzəri olaraq, məlum buz kristallarının sıfır entropiyasını eksperimental olaraq müəyyən etməkdən daha çox dəqiqliklə (qüsurları və enerji səviyyəsinin yayılmasını nəzərə almadan) hesablamaq mümkün olardı.

Toplu buzdakı protonların sırası nizamlanmasa da, səth yəqin ki, bu hissəciklərin asılmış H atomları və O-tək cütləri (sifariş edilmiş hidrogen bağları ilə sıfır entropiya) zolaqları şəklində düzülməsinə üstünlük verir. Sıfır nöqtəli pozğunluq ZPE, J ˣ mol -1 ˣ K -1 və başqaları tapılır. Yuxarıda göstərilənlərin hamısından buz üçün hansı növ kristal qəfəslərin xarakterik olduğu aydın və başa düşüləndir.






