Maddənin qazlı məcmu vəziyyətinin termodinamiği sistemlərdə termodinamik tarazlığı və kvazistatik keçidləri öyrənən fizikanın mühüm sahəsidir. Sistemlərin davranışı ilə bağlı proqnozların əsaslandığı əsas model ideal qaz modelidir. Onun istifadəsi ilə Mendeleyev-Klapeyron tənliyi əldə edilmişdir. Bunu məqalədə nəzərdən keçirin.
İdeal qaz
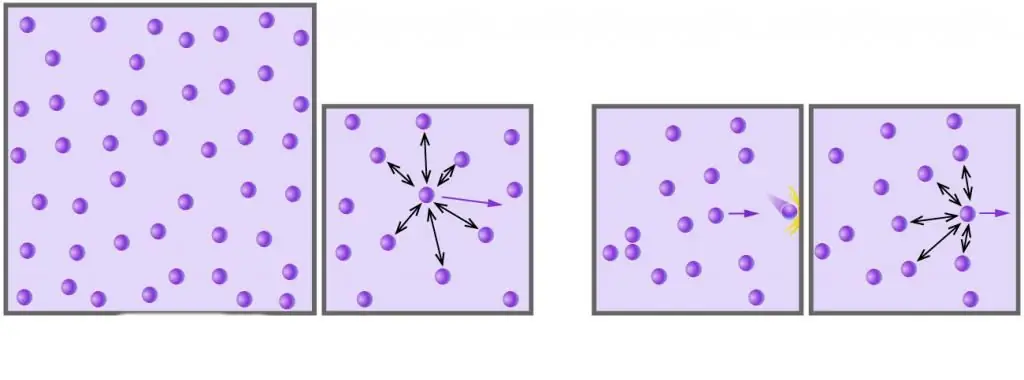
Bildiyiniz kimi, bütün real qazlar molekullardan və ya atomlardan ibarətdir, onların arasındakı məsafələr aşağı təzyiqlərdə ölçüləri ilə müqayisədə çox böyükdür. Bundan əlavə, yüksək temperaturda, mütləq miqyasda, molekulların kinetik enerjisi zəif dipol-dipol qarşılıqlı təsirləri ilə əlaqəli potensial enerjisini üstələyir (əgər bu qarşılıqlı təsirlərə əlavə olaraq, digər kimyəvi bağlar, məsələn, ion və ya hidrogen, sonra daxili sistem enerjisinin potensial komponentinə əhəmiyyətli töhfə verirlər).
GörəNormala yaxın şəraitdə bir çox real qazlar üçün onların daxili qarşılıqlı təsirlərini və hissəcik ölçülərini nəzərə almamaq olar. Bu iki əsas təxmin ideal qaz modelini təşkil edir.
Fizikada Mendeleyev tənliyi

Bu tənliyi Klapeyron-Mendeleyev qanunu adlandırmaq daha düzgün və ədalətlidir. Fakt budur ki, ilk dəfə 1834-cü ildə fransız mühəndis Emil Klapeyron tərəfindən qeydə alınıb. O, bunu 19-cu əsrin əvvəllərində kəşf edilmiş Boyle-Mariotte, Gay-Lussac və Charles qaz qanunlarını təhlil edərək etdi.
Rus kimyaçısı Dmitri Mendeleyevin ləyaqəti ondadır ki, o, tənliyə müasir və istifadəsi asan riyazi forma verib. Xüsusilə, Mendeleyev tənliyə bütün qazlar üçün sabiti daxil etdi R=8, 314 J/(molK). Klapeyron özü hesablama prosesini çətinləşdirən bir sıra empirik sabitlərdən istifadə etdi.
Mendeleyev-Klapeyron tənliyi aşağıdakı kimi yazılır:
PV=nRT.
Bu bərabərlik o deməkdir ki, ifadənin sol tərəfindəki təzyiq P və həcmi V hasil həmişə mütləq T temperaturun hasilinə və sol tərəfdəki n maddəsinin miqdarına mütənasibdir.
Tədqiq olunan ifadə dörd parametrdən ikisini düzəltsəniz, istənilən qaz qanununu əldə etməyə imkan verir. İzoproseslər zamanı ətraf mühitlə maddə mübadiləsinin olmadığı qapalı sistemlər öyrənilir (n=const). Bu proseslər tək sabit termodinamik parametr (T, P və ya V) ilə xarakterizə olunur.

Nümunə problem
İndi isə Mendeleyev-Klapeyron tənliyi üzrə məsələni həll edək. Məlumdur ki, 500 qram ağırlığında olan oksigen 2 atmosfer təzyiqində 100 litr həcmli silindrdə olur. Sistemin termodinamik tarazlıqda olduğunu nəzərə alsaq, şardakı temperatur nə qədərdir.
Xatırladaq ki, tərifə əsasən, maddənin miqdarı düsturla hesablanır:
n=m/M.
Burada m sistemin bütün hissəciklərinin kütləsi, M onların orta molyar kütləsidir. Bu bərabərlik Mendeleyev tənliyini aşağıdakı formada yenidən yazmağa imkan verir:
PV=mRT/M.
Bu tapşırığın iş düsturunu haradan əldə edirik:
T=PVM/(mR).
Bütün kəmiyyətləri SI vahidlərinə çevirmək və onları bu ifadə ilə əvəz etmək qalır:
T=21013250, 10, 032/(0, 58, 314)=156 K.
Hesablanmış temperatur -117 oC. Bu temperaturda oksigen hələ də qaz halında olsa da (-182,96 oC-də kondensasiya olunur), belə şəraitdə ideal qaz modeli yalnız hesablanmış dəyərin keyfiyyətcə qiymətləndirilməsini əldə etmək üçün istifadə edilə bilər.






