Fizikada termodinamik sistemlərin tədqiqində mühüm suallardan biri də bu sistemin hansısa faydalı işi yerinə yetirə biləcəyi sualıdır. İş anlayışı ilə sıx bağlı olan daxili enerji anlayışıdır. Bu yazıda biz ideal qazın daxili enerjisinin nə olduğunu nəzərdən keçirəcəyik və onun hesablanması üçün düsturlar verəcəyik.
İdeal qaz
Qaz haqqında xarici təsir altında heç bir elastik qüvvəyə malik olmayan və nəticədə həcmini və formasını saxlamayan yığılma vəziyyəti kimi hər bir məktəbli bilir. Çoxları üçün ideal qaz anlayışı anlaşılmaz və qeyri-müəyyən olaraq qalır. Gəlin bunu izah edək.
İdeal qaz aşağıdakı iki vacib şərti ödəyən istənilən qazdır:
- Onu təşkil edən hissəciklərin ölçüsü yoxdur. Onların ölçüləri var, lakin aralarındakı məsafələrlə müqayisədə o qədər kiçikdir ki, bütün riyazi hesablamalarda bunu nəzərə almamaq olar.
- Zərrəciklər van der Waals qüvvələri və ya qüvvələrindən istifadə edərək bir-biri ilə qarşılıqlı təsir göstərmirbaşqa təbiət. Əslində, bütün real qazlarda belə qarşılıqlı təsir mövcuddur, lakin onun enerjisi kinetik hissəciklərin orta enerjisi ilə müqayisədə cüzidir.
Təsvir olunan şərtləri temperaturları 300 K-dən yuxarı olan və təzyiqləri bir atmosferdən çox olmayan demək olar ki, bütün real qazlar təmin edir. Çox yüksək təzyiqlər və aşağı temperaturlar üçün qazların ideal davranışdan sapmasını müşahidə edir. Bu vəziyyətdə real qazlardan danışılır. Onlar van der Waals tənliyi ilə təsvir edilmişdir.
İdeal qazın daxili enerjisi anlayışı
Tərifə uyğun olaraq, sistemin daxili enerjisi bu sistemin daxilində olan kinetik və potensial enerjilərin cəmidir. Bu konsepsiya ideal qaza tətbiq edilərsə, potensial komponent atılmalıdır. Həqiqətən də, ideal qazın zərrəcikləri bir-biri ilə qarşılıqlı əlaqədə olmadığı üçün onları mütləq vakuumda sərbəst hərəkət edən hesab etmək olar. Tədqiq olunan sistemdən bir hissəciyi çıxarmaq üçün daxili qarşılıqlı təsir qüvvələrinə qarşı iş görmək lazım deyil, çünki bu qüvvələr mövcud deyil.
Beləliklə, ideal qazın daxili enerjisi həmişə onun kinetik enerjisi ilə üst-üstə düşür. Sonuncu, öz növbəsində, sistemin hissəciklərinin molar kütləsi, onların sayı, həmçinin tərcümə və fırlanma hərəkətinin orta sürəti ilə unikal şəkildə müəyyən edilir. Hərəkət sürəti temperaturdan asılıdır. Temperaturun artması daxili enerjinin artmasına səbəb olur və əksinə.
Formuladaxili enerji
İdeal qaz sisteminin daxili enerjisini U hərfi ilə işarələyin. Termodinamikaya görə o, sistemin H entalpiyası ilə təzyiq və həcm hasili arasındakı fərq kimi müəyyən edilir, yəni:
U=H - pV.
Yuxarıdakı paraqrafda biz müəyyən etdik ki, U dəyəri bütün qaz hissəciklərinin Ek ümumi kinetik enerjisinə uyğundur:
U=Ek.
Statistik mexanikadan, ideal qazın molekulyar kinetik nəzəriyyəsi (MKT) çərçivəsində belə çıxır ki, bir hissəciyin orta kinetik enerjisi Ek1 bərabərdir. aşağıdakı dəyər:
Ek1=z/2kBT.
Burada kB və T - Boltsman sabiti və temperaturu, z - sərbəstlik dərəcələrinin sayı. Ek sisteminin ümumi kinetik enerjisini Ek1 sistemdəki N hissəciklərinin sayına vurmaqla əldə etmək olar:
Ek=NEk1=z/2NkBT.
Beləliklə, ideal qazın daxili enerjisinin mütləq temperatur və qapalı sistemdəki hissəciklərin sayı baxımından ümumi formada yazılmış düsturunu əldə etdik:
U=z/2NkBT.
Monatomik və çox atomlu qaz
Məqalənin əvvəlki bəndində yazılmış U üçün düstur onun praktik istifadəsi üçün əlverişsizdir, çünki N hissəciklərinin sayını müəyyən etmək çətindir. Bununla belə, n maddəsinin miqdarının tərifini nəzərə alsaq, bu ifadəni daha əlverişli formada yenidən yazmaq olar:
n=N/NA; R=NAkB=8, 314 J/(molK);
U=z/2nR T.
Sərbəstlik dərəcələrinin sayı z qazı təşkil edən hissəciklərin həndəsəsindən asılıdır. Beləliklə, bir atomlu bir qaz üçün, z=3, çünki bir atom müstəqil olaraq fəzanın yalnız üç istiqamətində hərəkət edə bilər. Əgər qaz ikiatomikdirsə, onda z=5 olur, çünki üç tərcümə sərbəstlik dərəcəsinə daha iki fırlanma sərbəstliyi əlavə olunur. Nəhayət, hər hansı digər çox atomlu qaz üçün z=6 (3 tərcümə və 3 fırlanma sərbəstlik dərəcəsi). Bunu nəzərə alaraq, bir atomlu, iki atomlu və çox atomlu ideal qazın daxili enerjisi üçün düsturları aşağıdakı formada yaza bilərik:
U1=3/2nRT;
U2=5/2nRT;
U≧3=3nRT.
Daxili enerjini təyin etmək üçün tapşırıq nümunəsi
100 litrlik silindrdə 3 atmosfer təzyiqdə təmiz hidrogen var. Hidrogenin verilmiş şərtlərdə ideal qaz olduğunu fərz etsək, onun daxili enerjisinin nə olduğunu müəyyən etmək lazımdır.

U üçün yuxarıdakı düsturlar maddənin miqdarını və qazın temperaturunu ehtiva edir. Problemin vəziyyətində, bu miqdarlar haqqında tamamilə heç bir şey deyilmir. Problemi həll etmək üçün universal Klapeyron-Mendeleyev tənliyini xatırlamaq lazımdır. Şəkildə göstərilən görünüşə malikdir.
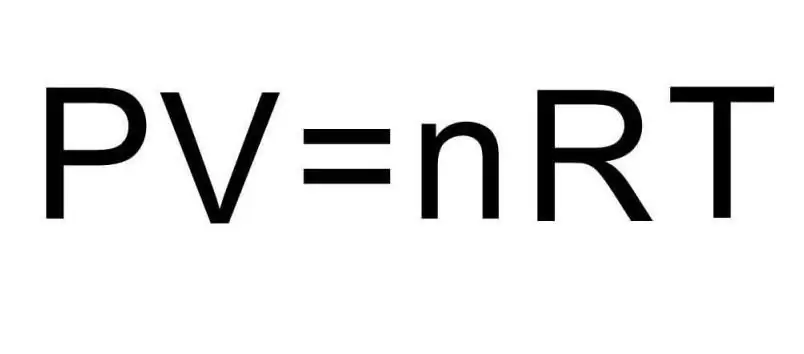
Hidrogen H2 iki atomlu molekul olduğundan daxili enerjinin düsturu belədir:
UH2=5/2nRT.
Hər iki ifadəni müqayisə edərək, problemin həlli üçün son düstura gəlirik:
UH2=5/2PV.
Təzyiq və həcm vahidlərini vəziyyətdən SI vahidlər sisteminə çevirmək, UH2 formulunda müvafiq dəyərləri əvəz etmək və əldə etmək qalır. cavab: UH2 ≈ 76 kJ.






